एक गैर-ध्रुवीय सहसंयोजक बंधन तब होता है जब परमाणु समान रूप से इलेक्ट्रॉनों को साझा करते हैं, और इलेक्ट्रॉन किसी भी परमाणु के आसपास अधिक समय नहीं बिताते हैं। एक ऑक्सीजन गैस (O2) अणु में एक गैर-ध्रुवीय सहसंयोजक बंधन होता है।
किस अणु में गैर-ध्रुवीय सहसंयोजक बंधन होता है?
एक गैर-ध्रुवीय सहसंयोजक बंधन का एक उदाहरण दो हाइड्रोजन परमाणुओं के बीच का बंधन है क्योंकि वे समान रूप से इलेक्ट्रॉनों को साझा करते हैं। एक गैर-ध्रुवीय सहसंयोजक बंधन का एक और उदाहरण दो क्लोरीन परमाणुओं के बीच का बंधन है क्योंकि वे समान रूप से इलेक्ट्रॉनों को साझा करते हैं।
निम्नलिखित में से किसके पास एक गैर-ध्रुवीय सहसंयोजक है?
लेकिन CH3CH3 में, C (2.5) और H(2.1) की इलेक्ट्रोनगेटिविटी लगभग समान है, अर्थात बंधित परमाणुओं के बीच इलेक्ट्रॉनों का समान बंटवारा किया गया है। इस प्रकार दिए गए अणुओं में से, CH3CH3 गैर-ध्रुवीय सहसंयोजक बंधन बनाते हैं।
क्या CO2 एक गैर-ध्रुवीय सहसंयोजक बंधन है?
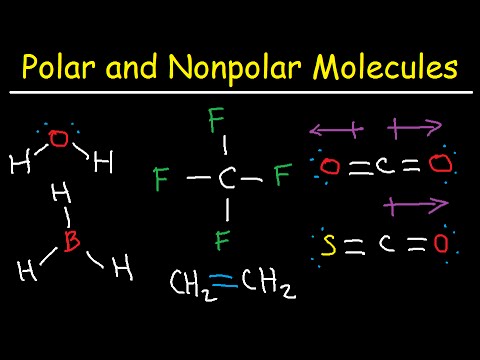
एक से अधिक प्रकार के सहसंयोजक बंधित अधातु परमाणुओं से बने अणु, जैसे कार्बन डाइऑक्साइड गैस (CO2), अध्रुवीय रहते हैं यदि वे सममित हैं या यदि उनके परमाणुओं में अपेक्षाकृत समान खिंचाव है. हेक्सेन गैसोलीन (C6H14) जैसे बड़े यौगिक भी सममित और गैर-ध्रुवीय होते हैं।
सहसंयोजक वर्ण का सही क्रम कौन सा है?
दिए गए अणुओं में हम देख सकते हैं कि प्रत्येक अणु से जुड़ा आयन एक ही है यानी क्लोरीन लेकिन धनायन अलग हैं। और धनायनों की विद्युत ऋणात्मकता का क्रम इस प्रकार है: ${text{Na < Li < Be}}$। तो सहसंयोजक वर्ण का बढ़ता क्रम होगा: ${text{NaCl < LiCl < BeC}}{{text{l}}_2}$