एनिलिन साइक्लोहेक्सिलामाइन की तुलना में कमजोर आधार क्यों है? एनिलिन में (C6HNH2 ), फिनाइल समूह (C 6H5) एक इलेक्ट्रॉन निकालने वाला समूह है और इसलिए नाइट्रोजन पर इलेक्ट्रॉन की उपलब्धता कम हो जाती है - NH2 समूह और इस प्रकार इसे कमजोर आधार बनाता है।
एनिलिन कमजोर आधार क्यों है?
एनिलिन अनिलिनियम आयन बनाने के लिए अनिच्छा से केवल एक प्रोटॉन स्वीकार करता है, और इसलिए एक कमजोर आधार है। जब एक -NH समूह एक स्निग्ध मूलक से जुड़ा होता है तो उसे कोई तुलनीय निरूपण स्थिरीकरण प्राप्त नहीं होता है। यह अपने नाइट्रोजन एकल युग्म पर एक प्रोटॉन को स्वीकार करने में कम अनिच्छुक है, और इसलिए स्निग्ध एमाइन मजबूत आधार हैं।
क्या एनिलिन साइक्लोहेक्सिलामाइन की तुलना में अधिक अम्लीय है?
प्रतिलेखित छवि पाठ: Cyclohexylamine एनिलिन की तुलना में अधिक बुनियादी है क्योंकि: एनिलिन कम हाइड्रोजन दान करने में सक्षम है। एनिलिन नाइट्रोजन पर इलेक्ट्रॉनों को सुगंधित वलय में कुछ हद तक निरूपित किया जाता है।
एनिलिन या साइक्लोहेक्सिलामाइन का मजबूत आधार कौन सा है?
साइक्लोहेक्सिलामाइन में, साइक्लोहेक्सिल समूह (गैर-सुगंधित) एक इलेक्ट्रॉन मुक्त करने वाला समूह है और इस प्रकार - NH2 के नाइट्रोजन पर इलेक्ट्रॉन घनत्व को बढ़ाता है।समूह और इसे एनिलिन (प्रेरक प्रभाव) से अधिक मजबूत आधार बनाता है।
एनिलिन अमोनिया की तुलना में कमजोर क्षार क्यों है?
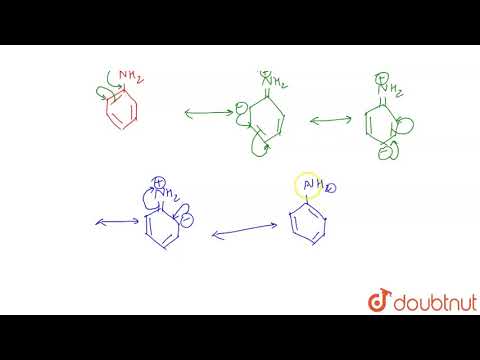
मूल रूप से, एनिलिन को सरलतम ऐरोमैटिक ऐमीन माना जाता है। … अब, एनिलिन को अमोनिया की तुलना में कमजोर क्षार माना जाता है। यह इस तथ्य के कारण है कि एनिलिन में अकेला जोड़ा बेंजीन रिंग के साथ अनुनाद में शामिल है और इसलिए NH3 में के रूप में दान के लिए उपलब्ध नहीं है।