विषयसूची:
- एसिटिक अम्ल में कौन-कौन से अंतराआण्विक बल मौजूद होते हैं?
- हाइड्रोक्लोरिक एसिड कौन सा अंतर-आणविक बल है?
- पानी और एसिटिक एसिड में अंतर-आणविक बल क्या हैं?
- एथेनोइक अम्ल द्विध्रुव द्विध्रुव है?

वीडियो: क्लोरोएसेटिक अम्ल में अंतराआण्विक बल?
2024 लेखक: Fiona Howard | [email protected]. अंतिम बार संशोधित: 2024-01-10 06:37
क्लोरोएसेटिक एसिड, क्योंकि लंदन फैलाव बल लंदन फैलाव बल लंदन फैलाव बल (LDF, जिसे फैलाव बल, लंदन बल, तात्कालिक द्विध्रुवीय-प्रेरित द्विध्रुवीय बल, उतार-चढ़ाव प्रेरित द्विध्रुवीय बांड या वैन के रूप में शिथिल रूप से जाना जाता है) डेर वाल्स बल) एक प्रकार का बल है जो परमाणुओं और अणुओं के बीच कार्य करता है जो सामान्य रूप से विद्युत रूप से सममित होते हैं; यानी इलेक्ट्रॉन हैं … https://en.wikipedia.org › विकी › London_dispersion_force
लंदन फैलाव बल - विकिपीडिया
इसके अणुओं मेंकमजोर हैं। क्लोरोएसेटिक एसिड, क्योंकि इसके अणुओं के बीच द्विध्रुवीय बल कमजोर होते हैं। आयोडोएसेटिक एसिड, क्योंकि लंदन के अणुओं के बीच फैलाव बल अधिक मजबूत होते हैं।
एसिटिक अम्ल में कौन-कौन से अंतराआण्विक बल मौजूद होते हैं?
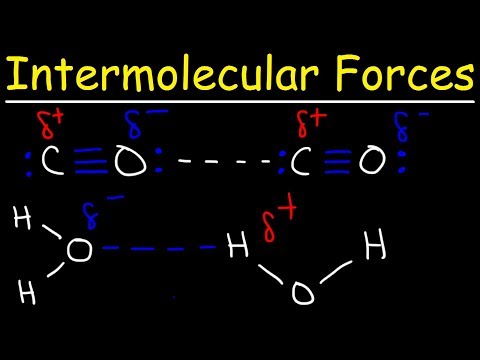
एसिटिक एसिड में (रासायनिक सूत्र $C{{H}_{3}}COOH$) में, इसमें तीन प्रकार के अंतर-आणविक बल होते हैं- हाइड्रोजन बंधन, द्विध्रुवीय-द्विध्रुवीय अंतःक्रियाएं और फैलाव बल। इसमें विशेष रूप से मजबूत प्रकार की हाइड्रोजन बॉन्डिंग होती है।
हाइड्रोक्लोरिक एसिड कौन सा अंतर-आणविक बल है?
एचसीएल में दो अंतर-आणविक बल मौजूद हैं: द्विध्रुवीय-द्विध्रुवीय और लंदन फैलाव बल। दोनों में से द्विध्रुव-द्विध्रुवीय बल अधिक प्रबल होते हैं। द्विध्रुव-द्विध्रुवीय बल H-Cl आबंध द्विध्रुव से उत्पन्न होते हैं (क्योंकि Cl, H से अधिक विद्युत ऋणात्मक है)।
पानी और एसिटिक एसिड में अंतर-आणविक बल क्या हैं?
पानी में मजबूत हाइड्रोजन बांड हैं। पानी की तरह, एसिटिक एसिड में मजबूत हाइड्रोजन बांड होते हैं। ठोस एसिटिक एसिड में, अणु हाइड्रोजन बांड से जुड़े चक्रीय जोड़े बनाते हैं।
एथेनोइक अम्ल द्विध्रुव द्विध्रुव है?
एसिटिक एसिड (CH3COOH) में, हाइड्रोजन बॉन्डिंग, द्विध्रुवीय-द्विध्रुवीय अन्योन्यक्रिया और फैलाव बल मौजूद होते हैं जबकि कार्बन टेट्राक्लोराइड में (CCl4) केवल फैलाव गैर-ध्रुवीय बल मौजूद हैं।
सिफारिश की:
क्या हाइड्रोक्लोरिक अम्ल एक प्रबल अम्ल है?

HCl एक मजबूत अम्ल है क्योंकि यह लगभग पूरी तरह से अलग हो जाता है। इसके विपरीत, एसिटिक एसिड जैसा कमजोर एसिड (CH 3 COOH) पानी में अच्छी तरह से अलग नहीं होता है - कई H + आयन भीतर बंधे रहते हैं अणु। हाइड्रोक्लोरिक एसिड इतना मजबूत एसिड क्यों है?
द्विध्रुवीय अंतराआण्विक बल हैं?

द्विध्रुव-द्विध्रुवीय अन्योन्यक्रियाएं दो अणुओं के बीच अंतर-आणविक आकर्षण-आकर्षण का एक प्रकार है … एक विद्युत मोनोपोल एक एकल आवेश होता है, जबकि एक द्विध्रुव दो विपरीत आवेश होते हैं जो प्रत्येक के निकट दूरी पर होते हैं। अन्य। अणु जिनमें द्विध्रुव होते हैं, ध्रुवीय अणु कहलाते हैं और प्रकृति में बहुत प्रचुर मात्रा में होते हैं। पांच प्रकार के अंतर-आणविक बल क्या हैं?
क्या सांद्र अम्ल प्रबल अम्ल होते हैं?

एक मजबूत एसिड वह है जो जलीय घोल में H3O+ आयन बनाने के लिए पूरी तरह से अलग हो जाता है, जबकि एक कमजोर एसिड केवल आंशिक रूप से ऐसा करता है। दूसरी ओर, एक सांद्र अम्ल वह है जिसमें जलीय घोल में H3O+ आयनों की बहुत अधिक सांद्रता होती है। मजबूत अम्ल सांद्र अम्ल से किस प्रकार भिन्न है?
क्लोरोएसेटिक एसिड अधिक अम्लीय क्यों होता है?

प्रश्न: क्लोरोएसेटिक एसिड एसिटिक एसिड की तुलना में अधिक अम्लीय क्यों है? उत्तर: क्लोरोएसेटिक एसिड अधिक मजबूत होता है, क्योंकि इसमें (कम विद्युतीय) हाइड्रोजन परमाणुओं के स्थान पर (अधिक विद्युतीय) क्लोरीन परमाणु होते हैं। क्लोरोएसेटिक एसिड एसिटिक एसिड की तुलना में अधिक अम्लीय क्यों है?
क्या अम्ल को अम्ल बनाता है?

अम्ल एक पदार्थ है जो हाइड्रोजन आयन देता है इस वजह से जब कोई एसिड पानी में घुल जाता है तो हाइड्रोजन आयन और हाइड्रॉक्साइड आयन हाइड्रॉक्साइड आयनों के बीच संतुलन बना रहता है Hydroxide रासायनिक सूत्र OH − के साथ एक द्विपरमाणुक आयन है इसमें एक ऑक्सीजन और हाइड्रोजन परमाणु होते हैं जो एक एकल सहसंयोजक बंधन द्वारा एक साथ होते हैं, और एक नकारात्मक विद्युत आवेश वहन करते हैं। यह पानी का एक महत्वपूर्ण लेकिन आमतौर पर मामूली घटक है। यह एक आधार, एक लिगैंड, एक न्यूक्लियोफाइल और एक उत्प्रेरक






